脊索動物の温度適応を支える酵素進化の仕組みの一端を解明
― なぜ魚と人では酵素の働く温度が違うのか?その分子メカニズムを解明 ―
【発表論文】
“Hydrophobic interactions determine the optimum temperature of a housekeeping enzyme”
J. Biol. Chem. 302(3), 111234 (2026).
Yamamoto T., Shiraishi A., Sakai T., Wada A., Satake H.*
公益財団法人サントリー生命科学財団・生物有機科学研究所
Open access DOI:https://doi.org/10.1016/j.jbc.2026.111234
研究のポイント
- ・本研究は、生物が温度環境に適応して進化する仕組みの理解につながる成果です。
- ・脊椎動物に尾索動物(ホヤ)と頭索動物(ナメクジウオ)を加えた11種の脊索動物の酵素を比較し、酵素の至適温度がそれぞれの生物の体温と関係していることを明らかにしました。
- ・酵素の至適温度は、タンパク質内部の特定の構造間に形成される疎水性相互作用の数によって決まることを発見しました。
- ・これらの相互作用は主に4つのアミノ酸の配置によって形成されていることが分かりました。
- ・相互作用の数から酵素の至適温度を予測する数式を構築し、高い精度で予測できることを示しました。
■研究の背景
脊椎動物に尾索動物(ホヤ)と頭索動物(ナメクジウオ)を加えた脊索動物はそれぞれ異なる温度環境で生活しています。鳥類や哺乳類のように体温を一定に保つ恒温動物もいれば、魚類や両生類のように外部環境によって体温が変化する変温動物も存在します。
生物の体内では、エネルギー代謝など生命活動に不可欠な多くの酵素が働いています。これらの酵素は進化の過程で広く保存されている一方、それぞれの生物の体温に適した温度で最も効率よく働くことが知られています。しかし、同じ酵素でありながら、生物種によって働きやすい温度が異なる理由や、その分子メカニズムはこれまでほとんど分かっていませんでした。 そこで本研究では、様々な生物が持っている酵素(ハウスキーピング酵素)かつエネルギー代謝に重要なであるアデニル酸キナーゼ1(AK1)に着目し、脊索動物における酵素の至適温度がどのような仕組みで決まるのかを調べました。
■研究の成果
本研究では、11種の脊索動物のAK1酵素を解析し、それぞれの酵素が最も活発に働く温度(至適温度)を測定しました。その結果、AK1の至適温度は各生物の体温と密接に関係していることが明らかになりました。
さらに、タンパク質構造を詳細に解析したところ、酵素の至適温度はアミノ酸配列の類似性では説明できず、タンパク質内部の特定の構造間に形成される疎水性相互作用の数と強く関係していることが分かりました。特に、酵素の第4構造領域と第17構造領域の間に形成される疎水性相互作用が、至適温度を決定する重要な要因であることが示されました。
これらの疎水性相互作用は主に4つのアミノ酸(Ile12、Phe14、Phe107、Ile111)の配置によって形成されていることが分かりました。これらのアミノ酸自体は多くの脊索動物で保存されていますが、その周囲の構造環境の違いによって相互作用の数が変化し、結果として酵素の至適温度が変化すると考えられます。
さらに研究チームは、疎水性相互作用の数から酵素の至適温度を予測する数式を構築しました。この数式により、脊索動物のAK1の至適温度を最大±1.7℃の誤差で予測できることが示されました。
また、酵素の構造の一部を別の生物のものと入れ替えた変異体を作製したところ、疎水性相互作用の数が変化すると酵素の至適温度も変化することが確認され、この相互作用が酵素の温度特性を決定する重要な要因であることが実験的に証明されました。
■まとめと今後の展望
本研究により、脊索動物のハウスキーピング酵素AK1において、タンパク質内部の疎水性相互作用の数が酵素の至適温度を決定する主要因であることが明らかになりました。
これらの結果は、生物が進化の過程でアミノ酸変異によってタンパク質内部の相互作用を調節し、それによって酵素の温度特性を変化させることで、さまざまな温度環境に適応してきた可能性を示しています。 今後は、このような温度特性の制御機構が、「脊索動物以外の動物」や「他の酵素」でも共通して存在するのかを調べることで、生物の温度適応の分子メカニズムの理解がさらに進むと期待されます。また、酵素の温度特性を予測・設計する技術として、産業用酵素の開発などバイオテクノロジー分野への応用も期待されます。
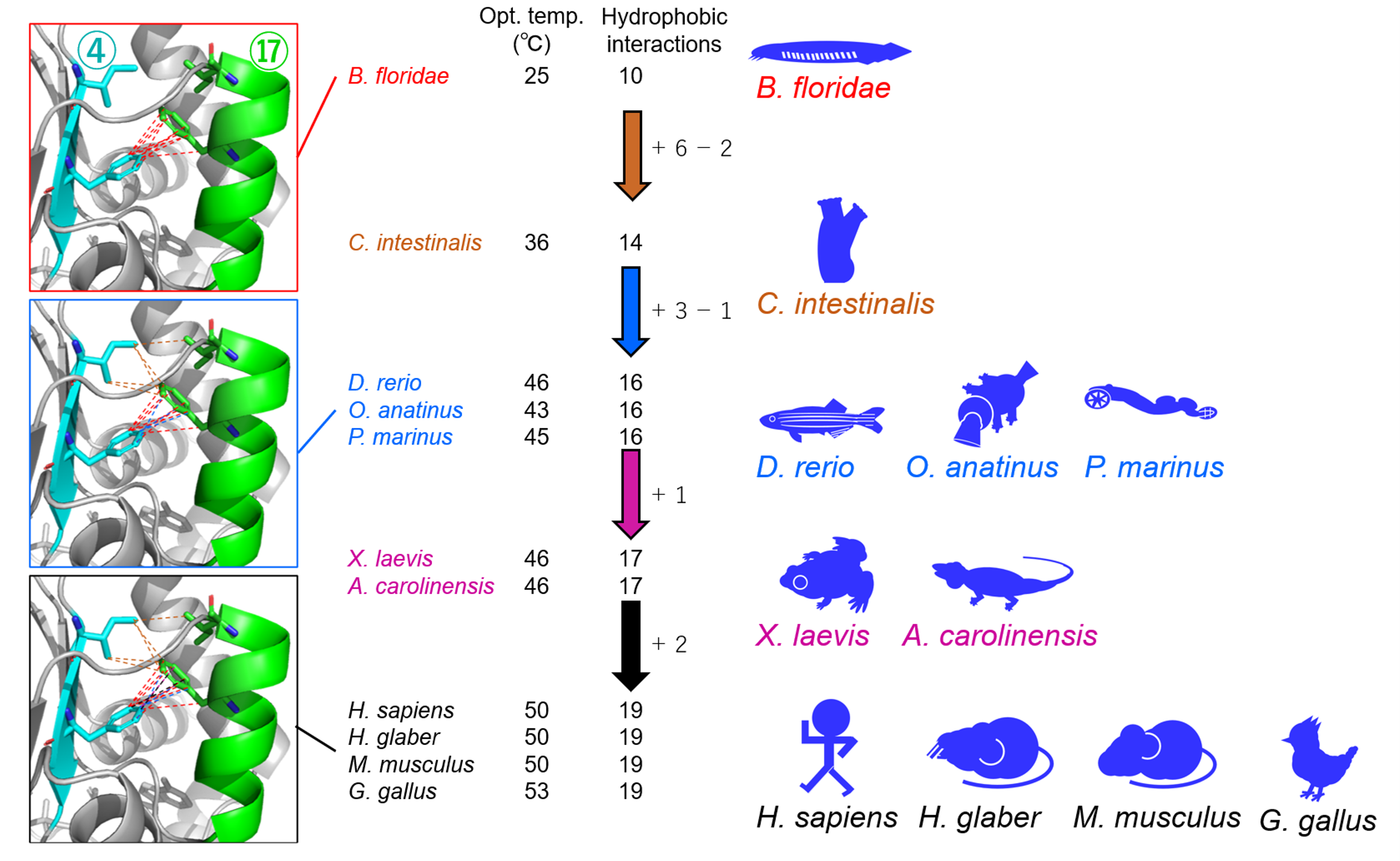
疎水性相互作用数と酵素至適温度の関係:④番目と⑰番目の二次構造間に形成される相互作用数が酵素の至適温度の大部分を決定することを発見し、この分子機構が多様な体温を生み出す進化的基盤となっていることを示した。
内容に関する問い合わせ先: 山本( ←Click )
